“Atomun Yapısı ve Geçmişten Günümüze Atom Modelleri” içeriği, 2018 Fen Bilimleri Öğretim Programı’na uygun olarak hazırlanmıştır. Aydınoloji ©
F.7.4.1. Maddenin Tanecikli Yapısı
Önerilen Süre: 6 ders saati
F.7.4.1.1. Atomun yapısını ve yapısındaki temel parçacıklarını söyler.
F.7.4.1.2. Geçmişten günümüze atom kavramı ile ilgili düşüncelerin nasıl değiştiğini sorgular.
a. Atom teorileri ile ilgili ayrıntıya girilmez.
b. Bilimsel bilginin zamanla değişebileceğine vurgu yapılır.
c. Bilimsel bilgi türlerinden teori hakkında genel bilgi verilir.
“Atomun Yapısı ve Geçmişten Günümüze Atom Modelleri” konusunu öğrenirsem ne kazanacağım? Günlük yaşamıma bir faydası olacak mı?
Bu içeriği okduğunda günümüzdeki atom modeline ulaşana kadar katedilen aşamalar ve bilimsel bilginin sorgulanabilir ve gelişime her an açık olduğunu göreceksin. Günlük yaşamında daha sorgulayıcı ve eleştirel bir bakış açısı kazanacaksın. Bilimsel bilgilerin sorgulanabilir ve sürekli gelişime açık olduğunu anlayacaksın.
Atom nedir?
Atom, bir elementin tüm özelliklerini taşıyan en küçük parçasıdır.
Atomun yapısında ne bulunur?
Atom, çok sayıda atomaltı parçacıktan oluşsa da ortaokulda bilmen gerken parçalar yalnızca proton, nötron ve elektrondur.
Proton nedir?
Atomun çekirdeğinde bulunan pozitif yüklü parçacıktır. Proton sayısı atoma kimlik kazandırır. Örneğin bir atomun çekirdeğinde 79 proton olduğunda, oda sıcaklığında oldukça sert bir metal olan altın, 80 proton olduğunda oda sıcaklığında sıvı bir metal olan cıva oluyor.
Nötron nedir?
Atomun çekirdeğinde protonlarla birlikte bulunan yüksüz (nötr) parçacıktır. Sayıca genellikle proton sayısına yakın miktarda bulunur. Kütlesi protonun kütlesine çok yakındır.
Elektron nedir?
Atomun çekirdeğinin etrafındaki elektron buluru içinde dolanan negatif yüklü parçacıktır. Kütlesi ihmal edilebilecek kadar küçüktür (proton kütlesinin yaklaşık 1836’da biri). Kimyasal tepkimelerde önemli rolleri bulunur.

Proton, nötron ve elektron arasındaki ilişki nedir?
Proton (p) ile, Nötron (n) ile ve elektron (é) ile gösterilir.
Proton sayısından elektron sayısını çıkarırsak atomun yükünü buluruz.
p – é = yük
Yük pozitif, nötr ya da negatif olabilir.
Proton sayısı ile nötron sayısını toplarsak atomun kütle numarasını (K.N) buluruz.
K.N = p + n
Aşağıdaki etkileşimli uygulamada atomu oluşturan parçacıkları gözlemleyebilirsin.
Bilimsel gelişim nedir?
Bilimsel gelişim, 100°C’ta kaynayacağını bildiğiniz halde suyu kaynatmak ve bunu doğrulamaktır. Bilimsel gelişim ispatlara ve sorgulara dayalıdır. Eğer herhangi bir bilimsel veriye inanmıyorsanız derhal test edip kendi gözlerinizle görebilirsiniz. Eğer testinizi doğru biçimde yapar ve bilimsel bilginin gerçek olmadığını kanıtlarsanız bilimsel gelişimi sağlamış olursunuz.
Bu içerikte amaç, atom modellerinin günümüzdeki hale gelişini anlatmaktan öte, bilimsel bir bilginin nasıl değişip gelişebileceğini göstermektir.
Atom düşüncesinin doğuşu nasıl başladı?
Yunan filozof Democritus (M.Ö. 460) , maddeler üzerine yaptığı incelemede gözleriyle görebileceğinden çok daha küçük parçalara ayrılabileceğiniz öngörmüş ve bunun sonsuza kadar devam edemeyeceği fikrini ilk defa ortaya atmıştır. Democritus’a göre ulaşılan son noktada bölünemeyecek bir parça olmalıdır ve bu parçaya “bölünemez” anlamına gelen “atomos” adını vermiştir. Günümüzde kullandığımız atom kelimesi de buradan türemiştir.

Democritus’a göre tüm maddeler aynı taneciklerden oluşuyordu. Ancak ona göre; demir, ahşap, taş, su, hava… vb. maddelerin yapısal farklılığına neden olan etken, taneciklerin birbirine göre dizilimi ve bütünleşik biçimde duran taneciklerin sayısıydı.
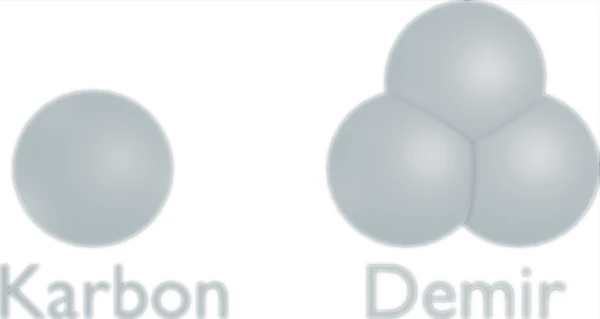
Democritus’un modeliyle ilgili bilmem gerekenler neler?
- Atom fikri ilk defa ortaya atıldı.
- Atom bölünemez.
- Farklı maddeler aynı atomların sayı ve diziliş farklılığından dolayı farklı olur.
- Bu görüş bilimsel değildir, çünkü bilimsellik ve deneysel bulgular değil, kişisel görüş esastır.
Dalton Atom Modeli

Dalton (John Dalton), 1805 yılında bugünün atom modelinin bilimsel başlangıcını yapmıştır. Dalton Modeli’ni önemli yapan nokta atom modeli üzerine yapılan ilk bilimsel çalışma olmasıdır.

Dalton Atom Modeli ile ilgili bilmem gerekenler neler?
- Atom üzerine ilk bilimsel çalışma bu atom modelinde yapılmıştır.
- Atom içi dolu “berk” küredir.
- Atom parçalanamaz.
- Farklı maddeler farklı cins atomlardan oluşmuştur.
Thomson Atom Modeli

İngiliz fizikçi Joseph John Thomson tarafından 1904 yılında ortaya atılmıştır. Thomson Atom Modeli’ni önemli yapan nokta ilk defa elektronlardan bahsedilmesidir.
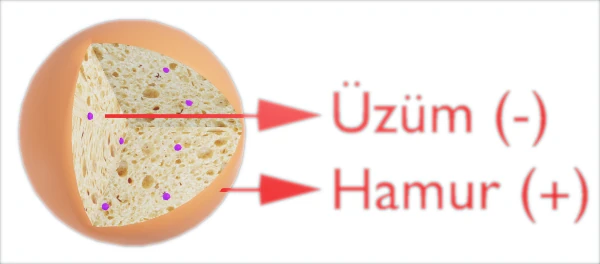
Thoson Atom Modeli ile ilgili bilmem gerekenler neler?
- İlk defa elektronlardan bahsedilmiştir.
- “Üzümlü Kek” modeli olarak da bilinir.
- Atomun berk kısmı pozitif ( + ) yüklüdür ve elektronlar negatif ( – ) yüklü olup berk içine dağılmıştır.
- Atomun berk kısmı kekin hamuruna, elektronlar ise üzümlere benzetilmiştir.
- Atom parçalanabilir.
Rutherford Atom Modeli

Rutherford Atom Modeli, 1911 yılında Ernest Rutherford tarafından ortaya atılmıştır. Bu modeli önemli yapan detay elektronların sürekli hareket halinde ve atomun çekirdeğinin dışında bulunduğu bulgusudur.
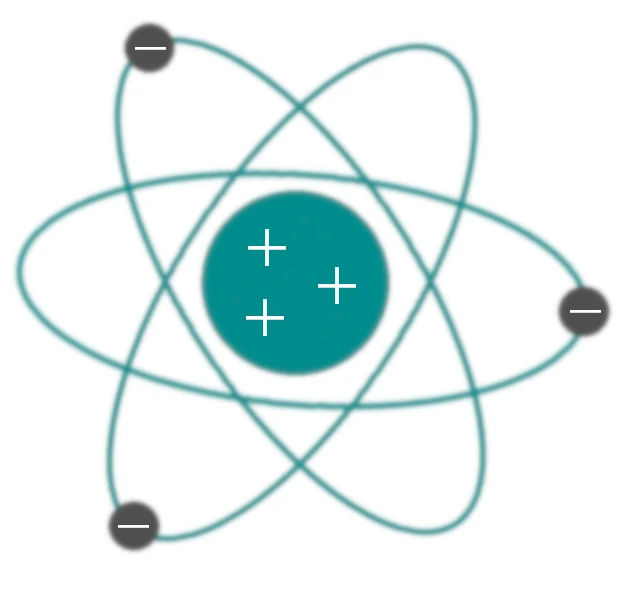
Rutherford Atom Modeli ile ilgili bilmem gerekenler neler?
- İlk defa elektronların hareketli olduğundan bahsedilmiştir.
- Atomu Güneş Sistemi’ne benzetmiştir.
- Atomun çekirdeği bir bütün halde küre şeklinde pozitif ( + ) yüklü bir parçacık olarak betimlenmiştir.
- Elektronlar ise belirli yörüngelerde dolanan hareketli ve nefatif ( – ) parçacıklar olarak betimlenmiştir.
Bohr Atom Modeli

Bohr Atom Modeli, Niels Henrik Bohr tarafından 1913 yılında ortaya atıdı. Bu modeli önemli yapan noktalar elektronların belirli enerji katmanlarında dolandığından bahsetmesidir. Ayrıca çekirdekte yüksüz nötronların da bulunduğunu belirtir.
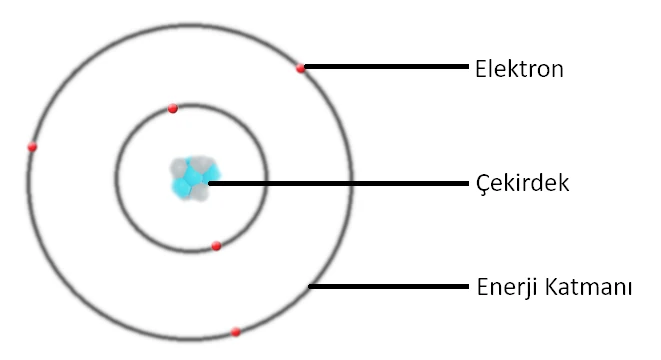
Bohr Atom Modeli ile ilgili bilmem gerekenler neler?
- Elektronlar çekirdeğe belirli uzaklıktaki katmanlarda dolanır.
- Her katman belirli sayıda elektron taşıyabilir.
- Eğer son katman maksimum elektron sayısına ulaşmışsa atoma eklenen elektron bir üst katmana yerleşir.
- Çekirdekte pozitif ( + ) yüklü proton ve yüksüz (nötr) nötron bulunur.
Bulut (Modern) Atom Teorisi

Modern Atom Teorisi olarak da bilinen bu modelin “teori” seviyesinde yani kanıtlanmış olmasının nedeni, atomun görüntüsü konusunda somut bir çalışmanın ürünü olmasıdır. Bir atom üzerine çok sayıda yavaşlatılmış atomaltı parçacık atışı yapılıyor ve bu parçacıklar elektronlarla çarpışarak karşı taraftaki film tabakasına ulaşamıyor. Atomun içinden çarpışma olmaksızın geçen atışlar film üzerinde yanmaya neden olarak bir iz oluşturuyor. Bu iz o bölgede elektronların çok görülmediği, az yanan bölümler ise elektronların çok görüldüğü bölge anlamına geliyor. Böylece elektronların yerlerini tahmini olarak elde edebiliyoruz.
Bunu röntgen çekilme işlemine benzetebilirsiniz. Röntgen filmi, üzerine gelen X ışınları nedeniyle farklılaşan bir malzeden yapılır. X ışınları yumuşak dokunuzdan kolaylıkla geçerken kemiklerinizin olduğu bölümden zor geçer ve ışığa tepki veren bu malzeme üzerinde, kemiklerinizin olduğu bölümlerle kemiksiz bölümler arasında fark oluşur. Bu fark iskeletinizin görüntüsüdür. Bulut Atom Teorisi de buna benzer bir yöntemle bulunduğu için somut delil kabul edilir ve böylece bir atom modeli ilk defa teori niteliği kazanmıştır.
Görsel 11’de gördüğünüz beyaz halkalar elektronların en çok görülebileceği bölgelerdir. Bulanık alanlar, elektronlara nadiren rastlanan alanardır. Yeşil alanlar ise elektronların hiç görülmediği alanlardır.
Tebrikler, konuyu tamamladın. Aşağıdaki kısa değerlendirmeyi çözerek öğrendiklerini test edebilirsin.
İnteraktif Etkinlik
Modelleri interaktif olarak incelemek istersen aşağıdaki interaktif etkinliği kullanabilirsin (Telefondaysan yan çevirip tam ekran yapabilirsin) Eğer donanımın buna uygun değilse ya da nasıl kullanacağını öğrenmek istiyorsan pencerenin aşağısındaki videodan etkinliği inceleyebilirsin.
Hipotez nedir?
Bir olayı aydınlatmak için yapılan test edilebilir tahminlere hipotez denir.
Teori nedir?
Test edilen hipotezler, doğrulanıp geniş bir bilgi ve kanıt temeline oturması durumunda, olayları açıklayan sistematik bir düşünce yapısı haline gelir. Bu duruma “teori” denir. Teori kanıtlanmış veridir.
Mola Zamanı
Atom Diyarı’nın Gizemi
Bir zamanlar, Bilim Diyarı’nın derinliklerinde, Atom Diyarı adında büyülü bir krallık vardı. Bu krallık, gözle görülemeyecek kadar küçük, ama bir o kadar da büyüleyici sırlarla doluydu. Atom Diyarı’nın gizemlerini çözmek için birçok cesur bilim insanı yola çıkmıştı.
Çok eski zamanlarda, Bilim Diyarı’nın bilge filozofu Democritus, bir gün sahilde kumdan kale yaparken kum tanelerini eline aldı ve düşündü: “Acaba bu kum tanelerini sonsuza kadar bölebilir miyim?” Democritus, her şeyin çok küçük, bölünemez parçacıklardan oluştuğunu hayal etti ve bu parçacıklara “atomos” adını verdi. Bu, Atom Diyarı’nın ilk keşfiydi ama o zamanlar sadece bir düşünceden ibaretti.

Yüzyıllar sonra Bilim Diyarı’nın cesur kaşifi John Dalton, Democritus’un hayalini gerçeğe dönüştürmeye başladı. Dalton, Atom Diyarı’ndaki atomların küçük, bölünemez küreler olduğunu ve her elementin kendine özgü atomları olduğunu öne sürdü. Bu, Atom Diyarı’nın ilk haritasıydı ve artık Atom Diyarı’nın nasıl fethedileceğinin stratejisi üzerine ilk adım atılmış oldu. Dalton’un atom modeli, farklı elementlerin nasıl birleşip bileşikler oluşturduğunu açıklamaya yardımcı oldu.

Atom Diyarı’nın Fethi Yaklaşıyor
Bu haritadan yola çıkan J.J. Thomson 1897’de acıktı ve üzümlü kek pişidi. Bilim Diyarı’nın dahi kaşifi J.J. Thomson, pişirdiği keki yerken Atom Diyarı’nın içinde daha küçük parçacıklar olduğunu keşfetti. Elektron adını verdiği bu negatif yüklü parçacıklar, tıpkı yemekte olduğu kekin içindeki üzümler gibi atomun içinde rastgele dağınık durumdaydı. Kekin hamuru pozitif, içindeki üzümler negatif yüklü elektronlar gibiydi. Bu model, Atom Diyarı’nın iç yapısını anlamada önemli bir adımdı. Bilim Diyarı savaşçıları, artık atomun iç yapısı hakkında daha fazla bilgi sahibiydi.

1911’de, Bilim Diyarı’nın cesur kaşifi Ernest Rutherford, Atom Diyarı’nın yapısını anlamak için altın bir levhaya atom altı parçacık gönderdiği ünlü deneyini yaptı. Beklenmedik bir şekilde bazı bazı parçacıklar levhanın arkasına geçmişti. Yok artık… Nasıl olur? Rutherford, Atom Diyarı’nın büyük kısmının boşluk olduğunu ve merkezinde pozitif yüklü küçük bir çekirdek bulunduğunu keşfetti. Elektronlar ise bu çekirdeğin etrafında dönüyordu. Bu model, Atom Diyarı’nın güneş sistemi gibi boşluklu yapıda olduğunu düşündürdü. Bu aslında çok ama çok büyük bir kazanımdı, artık Atom Diyarı’nın berk bir küre olmadığı elektronların serbestçe dolandığı fikri doğdu. Atom Diyarı’nın fethi çok yakındı, artık en büyük istihbarata sahipti Bilim Diyarı.

1913’te, Bilim Diyarı’nın dahi kaşifi Niels Bohr, Rutherford’un modelini geliştirerek elektronların belirli enerji seviyelerinde, yani katmanlarda döndüğünü öne sürdü. Bohr’un modeli, Atom Diyarı’nın enerji seviyelerini açıklamada büyük bir ilerlemeydi. Elektronlar, bu katmanlar arasında enerji alıp vererek yer değiştirebiliyordu.

Atom Diyarı’nın Fethi
Sonunda bütün çalışmalar sonuç verdi. 20. yüzyılın ortalarında, Bilim Diyarı’nın büyücüleri Werner Heisenberg ve Erwin Schrödinger, Atom Diyarı’nın yapısını derinlemesine incelemek için kuantum büyüsünü kullandı. “Kuantum Mekaniği” adı verilen bu büyülü bilim dalı, elektronların belirli yörüngelerde değil, olasılık bulutları içinde bulunduğunu gösterdi. Bu modern atom modeli, Atom Diyarı’nın karmaşık ve dinamik yapısını en iyi şekilde açıklayan modeldi. Üstelik bilimsel kanıtlara sahip olduğu için teori olmayı başarmıştı. Atom Diyarı Bilim Diyarı’nın yüzlerce yıl süren kararlı çabaları sonucu fethedilmişti.

Atom Diyarı’nın keşfi, Bilim Diyarı’nın cesur kaşifleri ve büyücüleri sayesinde yüzyıllar süren bir yolculuktu. Her yeni model, Atom Diyarı’nın gizemini biraz daha aydınlattı ve bugün bildiğimiz modern bilimin temellerini attı. Bu hikaye, bilimin nasıl sürekli geliştiğini ve her yeni keşfin bir öncekine dayandığını gösteriyor. Kim bilir, belki de sen de bir gün bu yolculuğa başlar ve Atom Diyarı’nın derinliklerinde saklı gizemleri keşfedersin.
Aşağıdaki ara değerlendirmeyi çözerek öğrendiklerini pekiştirebilirsin.
Yapay zekayla konuyu tartışmaya ne dersin?
Aşağıdaki yapay zeka sadece bu konu için özelleştirildi. Onunla konu hakkındaki düşüncelerini tartışabilirsin. Dikkat et, henüz gelişim aşamasında ve hata yapabilir. AR-GE çalışmaları için onunla konuşmalarını inceleyebileceğim, bu nedenle konuşurken özel bilgilerini vermemeni öneririm.
İçerik Sürümü: 1.1
Son Güncelleme: 16 Ağustos 2024
Kaynakça
Görseller
Görsel 9: https://upload.wikimedia.org/wikipedia/commons/5/55/Niels_Bohr_in_his_adolescent_years.jpg


Bir yanıt yazın